- Home
- /
- Nachrichten
- /
- Internationale Studie der JLU zeigt wie körpereigenes Schutzprogramm gegen Herzschwäche gezielt aktiviert werden kann
Internationale Studie der JLU zeigt wie körpereigenes Schutzprogramm gegen Herzschwäche gezielt aktiviert werden kann
Krankhafte Umbauprozesse im Herzen bremsen – wie dies möglich ist zeigt eine internationale Studie der JLU.

Mit dem CRISPRa-Ansatz gezüchtetes menschliches Herzmuskelgewebe wird verwendet, um die Auswirkungen einer KLF15-Aktivierung in molekularen und elektrophysiologischen Studien zu untersuchen. Bildnachweis: Johannes Peter Ruppert.
Neuer Ansatz gegen Herzschwäche: Ein internationales Forschungsteam hat eine neue Strategie vorgestellt, um das körpereigene Schutzprogramm gezielt wieder zu aktivieren und krankhafte Umbauprozesse im Herzen zu bremsen. Im Mittelpunkt steht eine spezielle CRISPR-Technologie, die Gene anschaltet, aber das Erbgut nicht schneidet. Mit Prof. Dr. Samuel Sossalla und Prof. Dr. Laura Zelarayán waren Forschende aus der Kardiologie der Justus-Liebig-Universität Gießen (JLU) und der Universitätsmedizin Göttingen (UMG) maßgeblich an der Publikation in der Zeitschrift „Signal Transduction and Targeted Therapy“ beteiligt.
Viele Formen der Herzschwäche entstehen nicht durch einen einzelnen Gendefekt. Stattdessen geraten in Herzmuskelzellen ganze Regulationsprogramme aus dem Gleichgewicht. Genau hier setzt die neue Studie an: Statt ein Gen zu ersetzen oder eine Mutation zu korrigieren, wollten die Forschenden ein natürliches Schutzprogramm der Zelle wiederherstellen. Grundlage dafür war die Identifikation des zentralen Regulators KLF15 als einem besonders wichtigen Schalter in gestressten Herzmuskelzellen.
Der Transkriptionsfaktor KLF15 ist ein Protein, das wichtige Schutz- und Stoffwechselprogramme im Herzmuskel steuert und die Herzmuskelzellen gesund und belastbar hält. Geht diese Steuerung verloren, werden krankheitsfördernde Programme aktiviert, während wichtige Stoffwechselprozesse aus dem Takt geraten. Nach den Ergebnissen der Studie ist KLF15 damit nicht nur ein Begleitfaktor, sondern ein entscheidender Knotenpunkt der zellulären Antwort auf chronischen Stress im Herzen. In der Studie zeigte sich, dass die Aktivität von KLF15 in krankhaft veränderten Herzmuskelzellen deutlich vermindert ist.
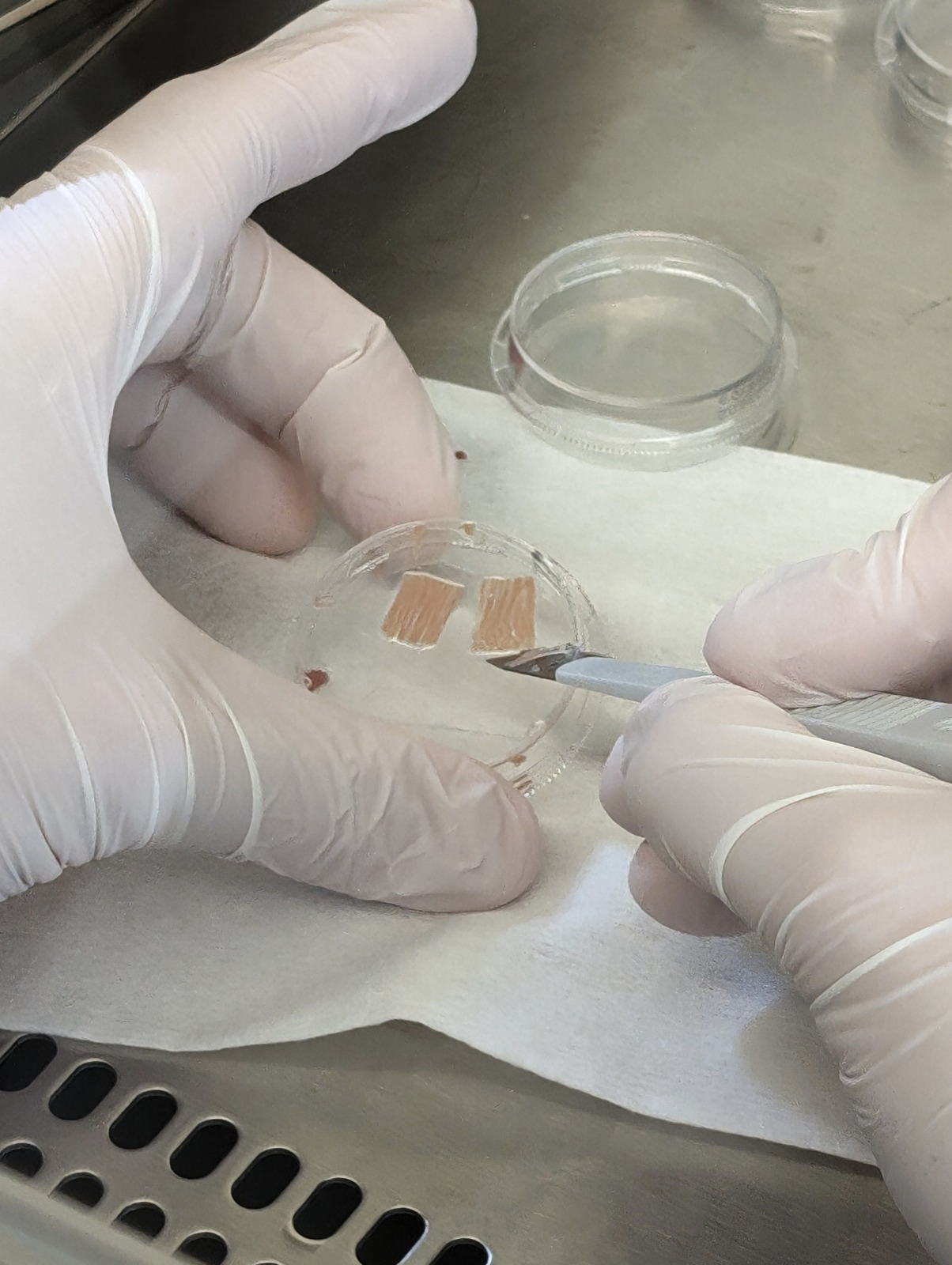
CRISPRa als neuer Hebel gegen Herzschwäche wird an menschlichem Herzgewebe untersucht. Bildnachweis: Johannes Peter Ruppert.
Mithilfe einer speziellen CRISPR-Technologie gelang es dem Team, die Aktivität dieses Gens gezielt zu steigern, ohne das Erbgut zu schneiden oder dauerhaft zu verändern. In den Untersuchungen schwächte dieser Ansatz krankhafte Stressreaktionen in Herzmuskelzellen ab und verringerte zudem Prozesse, die mit einer Vernarbung des Herzgewebes verbunden sind. Die Studie zeigt damit einen vielversprechenden neuen Weg auf: Statt einzelne Gene zu ersetzen, könnten künftig natürliche Schutzmechanismen des Herzens gezielt gestärkt werden.
Zusätzliche Untersuchungen an menschlichem Herzgewebe von Patientinnen und Patienten mit verschiedenen Formen der Herzmuskelerkrankung bestätigt die verminderte Menge des KLF15-Proteins. Die CRISPRa-Technologie konnte die KLF15-Expression in diesen Modellen erfolgreich korrigieren.
„Für die kardiovaskuläre Forschung an der JLU ist die Studie besonders bedeutsam, weil sie zeigt, wie sich moderne Genregulationstechnologien für komplexe Herzerkrankungen nutzen lassen“, betont Prof. Dr. Sossalla. „Unser Beitrag steht damit exemplarisch für einen Forschungsansatz, der molekulare Grundlagenforschung, translationale Herzmedizin und innovative Therapieentwicklung miteinander verbindet.“ Prof. Dr. Zelarayán ergänzt: „Gerade bei Herzschwäche, die häufig auf vielschichtigen Störungen der Genregulation beruht, eröffnet dieser Ansatz neue Perspektiven.“
Die Arbeit entstand in Zusammenarbeit mehrerer Standorte des Deutschen Zentrums für Herz-Kreislauf-Forschung (DZHK).
Publikation
Schoger, E., Kim, R., Bleckwedel, F. et al. Enhancing KLF15 activity in cardiomyocytes: a novel approach to prevent pathological reprogramming and fibrosis via nuclease-deficient dCas9VPR. Sig Transduct Target Ther 11, 76 (2026). https://doi.org/10.1038/s41392-026-02593-9
Kontakt
Justus-Liebig-Universität Gießen
Prof. Dr. med. Samuel Tobias Sossalla
Kardiologie
E-Mail: Samuel.Sossalla@innere.med.uni-giessen.de
Justus-Liebig-Universität Gießen
Prof. Dr. Laura Zelarayán
Kardiologie
E-Mail: laura.zelarayan-behrend@innere.med.uni-giessen.de